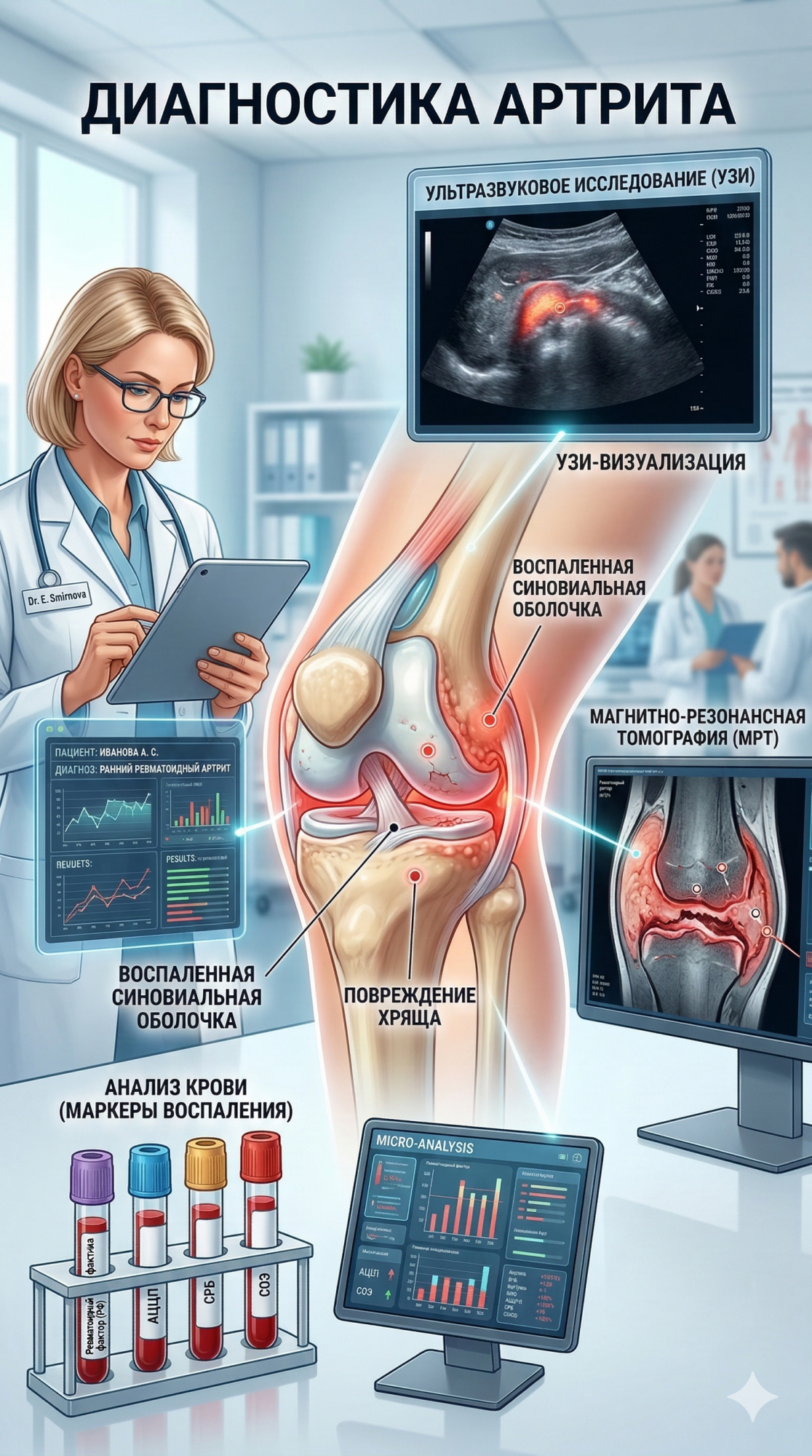
Современные методы диагностики артрита: анализы, УЗИ, МРТ — когда и какие исследования нужны
Эпидемиологический ландшафт и клиническое значение ранней верификации диагнозаРевматические заболевания на сегодняшний день представляют собой одну из наиболее значимых и масштабных проблем современного мирового здравоохранения, которая неуклонно снижает качество жизни миллионов пациентов и наносит колоссальный экономический ущерб государственным медицинским системам. В Российской Федерации ревматические патологии занимают уверенное второе место по распространенности среди взрослого населения, уступая лишь сердечно-сосудистым расстройствам. В структуре данных патологий традиционно доминируют остеоартрит, ревматоидный артрит, подагра и боли в нижней части спины, что в целом отражает глобальные эпидемиологические тенденции, характерные для большинства развитых западных стран. Однако при более детальном анализе наблюдаются и весьма специфические региональные паттерны, требующие пристального внимания научного сообщества. В частности, за последние двадцать пять лет распространенность ревматоидного артрита в российской популяции драматически увеличилась с 0,42% до 1%. Данный феномен, имеющий противоположный вектор по сравнению с некоторыми историческими данными прежних лет, связывают с целым комплексом факторов: глобальным старением населения, увеличением общей продолжительности жизни пациентов благодаря успехам терапии, а также неуклонно возрастающим влиянием негативных экологических факторов и коморбидных состояний, среди которых ведущую роль играют ожирение, сахарный диабет и артериальная гипертензия.
Понимание истинных масштабов проблемы существенно осложняется выраженным разрывом между официальной медицинской статистикой обращаемости и реальной популяционной заболеваемостью. Масштабные эпидемиологические исследования, охватившие выборку из 76 000 субъектов, проживающих в 18 различных регионах Российской Федерации, убедительно продемонстрировали, что статистические показатели, основанные исключительно на обращаемости пациентов в клиники, могут быть до пяти раз ниже реальной распространенности ревматических заболеваний. Абсолютно аналогичная, если не более тревожная, ситуация наблюдается и в отношении остеоартрита. При официально зарегистрированных четырех миллионах пациентов с установленным диагнозом в России, экстраполяция эпидемиологических данных позволяет с высокой долей уверенности предположить, что реальное число больных достигает пятнадцати миллионов человек. Заболеваемость остеоартритом демонстрирует стабильный и пугающий рост: ежегодно в России регистрируется около 600 000 новых случаев данной нозологии. В Курской области, население которой составляет 1,2 миллиона человек, симптоматический остеоартрит коленного сустава поражает 25% населения в возрастной группе от 38 до 95 лет. При этом более 50% пациентов с остеоартритом — это люди пожилого возраста с выраженными ограничениями физической активности и множественной коморбидностью, включающей ишемическую болезнь сердца и диабет
В свете столь пугающих эпидемиологических данных современные методы диагностики артрита играют критически важную, жизнеспасающую роль. Именно своевременная, прецизионная и высокоточная верификация патологии на самых ранних, доклинических или ранних клинических стадиях определяет долгосрочный прогноз, эффективность любого терапевтического вмешательства и фатальный риск инвалидизации пациента. Различия в клинической картине воспалительных артритов, включая существенные гендерные особенности манифестации симптомов и различную скорость прогрессирования, диктуют абсолютную необходимость персонализированного подхода, направленного на минимизацию времени от появления первых жалоб до постановки окончательного диагноза. Задержка между появлением симптомов и первой консультацией ревматолога остается серьезным препятствием на пути к достижению ремиссии. Многообразные методы диагностики артрита сегодня представляют собой сложный, многоуровневый алгоритм, в котором каждый следующий шаг логически вытекает из предыдущего, формируя целостную картину здоровья пациента
Патофизиологические основы и необходимость инновационного подхода
Патофизиология ревматоидного артрита и спондилоартритов отличается исключительной сложностью и многогранностью, вовлекая в деструктивный процесс механизмы аутоиммунной агрессии, дисрегуляции цитокиновой сети и аберрантных иммунных реакций. Ревматоидный артрит первично поражает синовиальную оболочку, вызывая ее гиперплазию и формирование паннуса, что в конечном итоге, при отсутствии адекватного лечения, неизбежно приводит к необратимой деструкции суставного хряща и субхондральной кости, обрекая пациента на тяжелую инвалидность. Спондилоартриты, включающие анкилозирующий спондилит и псориатический артрит, характеризуются более широким спектром поражения, затрагивая не только периферические, но и аксиальные суставы (позвоночник, крестцово-подвздошные сочленения), а также места прикрепления сухожилий к костям — энтезисы.Конвенциональные методы клинического обследования и устаревшие лабораторные алгоритмы на протяжении десятилетий демонстрировали недостаточную специфичность и чувствительность, что неизменно приводило к неприемлемым задержкам в постановке диагноза и, как следствие, к упущенному "окну терапевтических возможностей". Это терапевтическое окно — краткий период в начале заболевания, когда агрессивное медикаментозное вмешательство может полностью остановить прогрессирование болезни и индуцировать длительную безлекарственную ремиссию. Осознание этого факта привело к фундаментальному сдвигу в парадигме ревматологии: переходу к концепции "Treat-to-Target" (лечение до достижения цели), которая невозможна без идеальной диагностической базы. Современные методы диагностики артрита призваны решить именно эту задачу — выявить патологический процесс на молекулярном и микроструктурном уровне задолго до того, как произойдут необратимые анатомические изменения
Биохимический и иммунологический профиль: основа лабораторного поиска
Рассматривая базовые методы диагностики артрита, необходимо в первую очередь погрузиться в тонкости лабораторной диагностики, которая исторически и клинически формирует первичный фундамент для диагностического поиска ревматолога. Лабораторные исследования позволяют не только объективно подтвердить наличие системного или локального воспаления, но и надежно дифференцировать аутоиммунные процессы от дегенеративных изменений, таких как остеоартрит.В рутинной практике клиницисты первоначально опираются на оценку неспецифических маркеров острой фазы воспаления. Пациенты с активным ревматоидным артритом и другими воспалительными артропатиями почти всегда демонстрируют патологическое повышение скорости оседания эритроцитов (СОЭ) и значительный рост уровня С-реактивного белка (СРБ). Данные показатели биохимически отражают общую интенсивность воспалительного каскада в организме, реагируя на выброс провоспалительных интерлейкинов (таких как IL-6 и TNF-alpha) печенью. Однако клиницисты прекрасно осознают, что эти маркеры обладают крайне низкой нозологической специфичностью. Они могут реактивно повышаться при бактериальных и вирусных инфекциях, онкологических процессах, травмах и многих других системных патологиях. Следовательно, их изолированное использование для постановки диагноза абсолютно недопустимо.
Для точной и неоспоримой верификации ревматоидного артрита критическое, определяющее значение имеют высокоспецифические серологические аутоантитела. Согласно актуальным международным и российским рекомендациям, к основным диагностическим мишеням относятся ревматоидный фактор (РФ) и антитела к циклическому цитруллинированному пептиду (АЦЦП). Российские клинические рекомендации 2024 года по ведению ревматоидного артрита, официально одобренные Научно-практическим Советом Минздрава России и тщательно разработанные Ассоциацией ревматологов России, особо подчеркивают исключительную важность дополнительной иммунологической стратификации пациентов. В соответствии с этим документом, диагноз ревматоидного артрита в обязательном порядке должен дополняться указанием на статус АЦЦП: позитивный или негативный.
Антитела к циклическому цитруллинированному пептиду обладают высочайшей специфичностью (достигающей 95-98%) для ревматоидного артрита. Патофизиологически их появление связано с процессом цитруллинирования — посттрансляционной модификацией белков, при которой аминокислота аргинин превращается в цитруллин. При ревматоидном артрите иммунная система ошибочно распознает эти модифицированные белки как чужеродные и начинает вырабатывать против них антитела. Уникальная клиническая ценность АЦЦП заключается в том, что они могут обнаруживаться в сыворотке крови пациента за несколько лет до появления самых первых клинических симптомов поражения суставов. Это делает их абсолютно незаменимым инструментом предиктивной медицины, позволяющим выявлять лиц из группы высочайшего риска и начинать профилактические мероприятия или предельно раннюю терапию
Генетическое типирование и молекулярная диагностика в ревматологии
Помимо оценки гуморального иммунитета и выявления аутоантител, важнейшим и стремительно развивающимся аспектом современной лабораторной диагностики является генетическое типирование. Выявление специфического аллеля HLA-B27 с применением высокоточного метода полимеразной цепной реакции (ПЦР) служит основным, классическим иммуногенетическим маркером высокой индивидуальной предрасположенности к развитию тяжелых заболеваний из обширной группы серонегативных спондилоартритов. Биоматериалом для проведения данного сложного молекулярного анализа традиционно служит венозная кровь пациента.К группе спондилоартритов, генетически ассоциированных с носительством HLA-B27, относятся анкилозирующий спондилит (исторически известный как болезнь Бехтерева), псориатический артрит, реактивный артрит (возникающий после перенесенных урогенитальных или кишечных инфекций), синдром Рейтера, а также артриты, тесно ассоциированные с хроническими воспалительными заболеваниями кишечника (болезнь Крона, неспецифический язвенный колит), рецидивирующий передний увеит и некоторые формы ювенильного ревматоидного артрита. С точки зрения статистики и генетики, наличие в геноме антигена HLA-B27 увеличивает риск развития какого-либо заболевания из указанной группы приблизительно в двадцать раз по сравнению с лицами, не являющимися носителями данного гена.
Тем не менее, интерпретация результатов генетического тестирования требует от ревматолога высочайшего клинического мастерства и осторожности. Отрицательный результат анализа на HLA-B27 наблюдается у абсолютного большинства — 92-93% — здоровых представителей европейской популяции. Однако парадокс заключается в том, что этот же отрицательный результат встречается и у 10% пациентов с уже клинически и рентгенологически подтвержденным анкилозирующим спондилоартритом. Эти пациенты формируют особую, сложную для курации когорту лиц с так называемым HLA-B27-негативным спондилоартритом. Таким образом, важнейшее правило современной ревматологии гласит: отсутствие данного генетического маркера ни в коем случае не противоречит диагнозу и не может служить основанием для его снятия. Оно лишь требует более глубокой, комплексной оценки клинического статуса с обязательным и немедленным применением передовых методов аппаратной визуализации для поиска структурных подтверждений воспаления
Классическая рентгенография: историческая перспектива и современные реалии
Инструментальные методы диагностики артрита позволяют врачам визуализировать структурные изменения опорно-двигательного аппарата, обеспечивая жизненно необходимый переход от биохимической констатации факта системного воспаления к точной топографической и морфологической оценке локального поражения. Исторически самым первым и долгие годы единственным методом визуализации костных структур была традиционная рентгенография. В настоящее время рентгенологическое исследование все еще сохраняет свои позиции, но применяется преимущественно для ретроспективного стадирования заболевания и отслеживания динамики суставной деструкции в долгосрочной перспективе, на протяжении многих летРентгенография позволяет достоверно выявить сужение суставной щели (которое косвенно указывает на истончение гиалинового хряща), маргинальные (краевые) эрозии костной ткани, формирование остеофитов (костных разрастаний) и субхондральный склероз. Однако ее фундаментальным, неустранимым физическим недостатком в контексте задачи ранней диагностики является полная неспособность адекватно визуализировать мягкие ткани сустава. На рентгенограмме невозможно увидеть синовиальную оболочку, оценить структуру хряща, состояние связочного аппарата менисков и наличие воспалительного внутрисуставного выпота. Структурные повреждения костной ткани, которые становятся видимыми на рентгенограмме, фактически свидетельствуют о свершившихся, необратимых изменениях. В идеальной, современной клинической практике такие разрушения должны предотвращаться на гораздо более ранних этапах развития болезни с помощью своевременно назначенной таргетной терапии. Именно поэтому рентгенография уступила место инструментам более тонкой визуализации.
Ультразвуковое исследование: динамическая визуализация и энергетический допплер
Ультразвуковые методы диагностики артрита на сегодняшний день обладают неоспоримым клиническим преимуществом благодаря своей повсеместной доступности, относительной дешевизне, полному отсутствию вредного ионизирующего излучения и уникальной возможности проведения функциональных проб в режиме реального времени. Ультразвуковая диагностика позволяет неинвазивно, безболезненно и крайне быстро выявить первичные признаки воспалительных и дегенеративных изменений в суставах. К таким ранним признакам относятся синовит (патологическое утолщение синовиальной оболочки), наличие избыточного внутрисуставного выпота (жидкости), теносиновит (воспаление сухожильных влагалищ) и самые ранние, микроскопические краевые эрозии, которые еще физически не способны визуализироваться на классических рентгенограммахОсобую, выдающуюся диагностическую ценность в ревматологии представляет режим энергетического допплера (Power Doppler). Эта ультразвуковая технология позволяет с высокой точностью оценить степень васкуляризации, то есть патологического кровоснабжения и образования новых сосудов (неоангиогенеза) внутри гиперплазированной синовиальной оболочки. Степень васкуляризации, видимая на экране сканера как яркие цветовые локусы, напрямую и пропорционально коррелирует с активностью локального воспалительного процесса.
Для оценки истинной клинической эффективности ультразвука был проведен масштабный систематический обзор и метаанализ, результаты которого обобщили данные из баз MEDLINE, Embase и Web of Science с 1987 по март 2024 года. В исследование вошли 39 когортных исследований, включавших пациентов с так называемой клинически подозрительной артралгией — состоянием, при котором пациент испытывает воспалительные боли в суставах, но при мануальном осмотре врач еще не может пальпаторно определить явный клинический синовит. Из этого массива данных 26 исследований оценивали именно ультразвук, охватив грандиозную выборку в 6805 пациентов, из которых у 25% впоследствии развился ревматоидный или иной воспалительный артрит. Метаанализ показал, что регистрация сигнала энергетического допплера 1-й и более степени хотя бы в одном подозрительном суставе обладает чувствительностью в 37% (95% доверительный интервал 18%–60%) и впечатляющей специфичностью в 90% (95% ДИ 82%–94%) для точного прогнозирования будущего прогрессирования воспалительного артрита
Несмотря на столь высокую специфичность и клиническую пользу, УЗИ имеет ряд существенных, неустранимых физических ограничений. Ультразвуковая волна по законам акустики полностью отражается от плотных структур и не способна проникать сквозь кортикальный слой кости. Это делает принципиально невозможным оценку состояния внутрикостных структур и выявление отека костного мозга, который является одним из самых ранних и грозных предикторов аутоиммунной ревматологической патологии. Кроме того, УЗИ является в высшей степени операторозависимым методом: его диагностическая точность, чувствительность и специфичность критически, определяюще зависят от квалификации, мануальных навыков и клинического опыта специалиста, проводящего сканирование. Как отмечают исследователи, отсутствие единого консенсуса относительно пороговых значений для определения положительного результата УЗИ до сих пор ограничивает его стандартизацию. Метод также оказывается объективно менее информативным для четкой визуализации патологических тканей в анатомически труднодоступных участках (например, в крестцово-подвздошных сочленениях у тучных пациентов) и на самых ранних стадиях патологического процесса, безоговорочно уступая в этом отношении более сложным и совершенным квантовым технологиям.
Магнитно-резонансная томография: абсолютный стандарт детализированной визуализации
Выбирая высокотехнологичные методы диагностики артрита, ведущие специалисты мирового уровня все чаще отдают безоговорочное предпочтение магнитно-резонансной томографии (МРТ). МРТ абсолютно заслуженно считается непререкаемым золотым стандартом для комплексной, трехмерной оценки абсолютно всех компонентов сложного сустава, включая костный мозг, тончайший гиалиновый хрящ, мениски, внутри- и внесуставные связки, а также синовиальную ткань. Метод базируется не на проникающей радиации, а на явлении ядерного магнитного резонанса протонов водорода в сильном магнитном поле, что делает его абсолютно безопасным для многократного, регулярного применения в процессе динамического наблюдения за пациентом.Ключевым, революционным преимуществом МРТ перед всеми другими существующими инструментальными модальностями является ее уникальная способность выявлять отек костного мозга (остеит). Остеит — это патологическое скопление жидкости в губчатом веществе кости, которое является прямым предвестником будущих тяжелых костных эрозий. Этот феномен возникает за многие месяцы, а иногда и годы до появления первых клинических и классических рентгенологических признаков необратимой костной деструкции. При исследовании крупных сочленений, в частности в рамках коленного сустава, МРТ демонстрирует исключительные, недостижимые для других методов диагностические характеристики: чувствительность алгоритма достигает 96%, а специфичность приближается к абсолютной величине в 98%. Это делает МРТ безальтернативным методом выбора при клинической необходимости детализированного, скрупулезного обследования всех мягкотканных суставных и периартикулярных структур. Важнейшим аспектом является также то, что компьютерная, программная обработка сотен послойных изображений практически полностью минимизирует влияние человеческого фактора на начальном этапе сбора первичных данных, тем самым нивелируя риск операторских ошибок, свойственных мануальному ультразвуковому скринингу
В вышеупомянутом масштабном систематическом обзоре также оценивалась прогностическая роль МРТ у пациентов с клинически подозрительной артралгией. Было проанализировано 12 исследований, включавших 2782 пациента, из которых 19% впоследствии заболели ревматоидным артритом. Данные показали, что МРТ-визуализация синовита (даже если он присутствует всего в одном суставе) демонстрирует чувствительность 45% (95% ДИ 29%–62%) и специфичность 84% (95% ДИ 66%–94%) в прогнозировании последующего развития клинически развернутого воспалительного артрита
Более того, МРТ играет абсолютно незаменимую роль при ведении сложных, жизнеугрожающих клинических сценариев, таких как подозрение на острый септический (гнойный) артрит. Согласно авторитетным радиологическим руководствам, опубликованным для применения в 2025 году, расширенная визуализация с помощью МРТ (любого сустава верхней или нижней конечности) официально считается строгой медицинской необходимостью для диагностики и последующего ведения септического артрита в тех частых случаях, когда рутинная рентгенография, УЗИ или даже инвазивный артроцентез (диагностическая пункция сустава) оказываются недиагностическими или предоставляют информацию, недостаточную для определения экстренной тактики хирургического или антибактериального лечения. В тех редких ситуациях, когда МРТ физически не может быть выполнена, протокол рекомендует применение компьютерной томографии. Кроме того, именно МРТ является единственным адекватным инструментом в диагностике аксиального поражения (глубокого спондилита и сакроилиита) при псориатическом артрите и других серонегативных спондилоартропатиях, позволяя визуализировать активное воспаление в крестцово-подвздошных сочленениях и местах прикрепления связок (энтезитах) на самой ранней, дорентгенологической стадии, когда обычные снимки таза показывают абсолютную норму
Двухэнергетическая компьютерная томография в диагностике микрокристаллических артропатий
Специфические методы диагностики артрита, такие как двухэнергетическая компьютерная томография (ДЭКТ), открыли совершенно новую, невероятно точную эру в сложной дифференциальной диагностике микрокристаллических артропатий, и в первую очередь — подагры. Патофизиология классической подагры неразрывно связана с хроническим гиперурикемическим состоянием, которое приводит к преципитации и отложению кристаллов моноуратов натрия в синовиальной жидкости, хрящах, сухожилиях и периартикулярных тканях. Это, в свою очередь, провоцирует рецидивирующие приступы острого, невыносимо мучительного воспаления. Уникальность и гениальность технологии ДЭКТ заключается в ее способности использовать физический феномен различного поглощения рентгеновских лучей тканями при одновременном воздействии двух разных уровней энергии излучения (обычно 80 кВ и 140 кВ). Сложное программное обеспечение сканера анализирует эту разницу и позволяет с колоссальной точностью идентифицировать специфический химический состав исследуемой области, отделяя соли мочевой кислоты от кальцификатов или обычных костных структур.Двухэнергетическая КТ способна с феноменальной точностью определять объем, плотность и пространственно картировать количество и точную локализацию уратов в тканях сустава даже в так называемый межприступный период, когда пациент чувствует себя абсолютно здоровым и полностью отсутствуют какие-либо клинические признаки острого воспаления. Согласно самым последним, актуальным научным данным, данный высокотехнологичный вид исследования особенно эффективен и оправдан для визуализации тофусов (подагрических узлов, не видимых глазом) и строгого, объективного контроля эффективности уратснижающей терапии у людей с уже диагностированной и лечащейся подагрой. Тем не менее, в строго индивидуальном порядке и исключительно по решению опытного, высококвалифицированного лечащего врача-ревматолога, ДЭКТ может успешно применяться в качестве инновационного метода первичного тестирования при атипичном, неклассическом течении суставного синдрома. Этот подход особенно ценен тем, что позволяет избежать болезненной, инвазивной диагностической пункции мелких суставов (которая часто бывает технически сложной) с последующей поляризационной микроскопией синовиальной жидкости
Инновационные подходы: Искусственный интеллект и обработка естественного языка
Современная академическая медицина стремительно, беспрецедентными темпами интегрирует в свою повседневную клиническую и исследовательскую практику цифровые технологии высшего порядка. Передовые методы диагностики артрита уже сегодня включают широкое использование мощнейших алгоритмов искусственного интеллекта (ИИ) и машинного глубокого обучения. Эти технологии призваны окончательно преодолеть ограничения традиционных человеческих подходов. Одной из главных фундаментальных проблем конвенциональных методов обследования при ревматоидном артрите и спондилоартритах по-прежнему является недостаточная специфичность и чувствительность диагностических алгоритмов, что зачастую приводит к трагическим задержкам в постановке правильного диагноза и необратимому, разрушительному прогрессированию патологииИсследования в области передового машинного обучения активно ведутся для выявления абсолютно новых, неизвестных ранее транскриптомных биомаркеров на основе сложнейшего секвенирования РНК (RNA-seq). Ученые используют такие высокоуровневые математические алгоритмы, как Light Gradient Boosting Machine (LGBM), сверточные нейронные сети (CNN), метод опорных векторов (SVM), а также методы преодоления дисбаланса данных, такие как Synthetic Minority Over-sampling Technique (SMOTE). Автоматизированный анализ колоссальных профилей экспрессии тысяч генов позволяет с математической, безошибочной точностью дифференцировать тончайшие молекулярные механизмы, лежащие в основе различных аутоиммунных и аутовоспалительных процессов. Это открывает прямой, научно обоснованный путь к таргетной прецизионной терапии, которая будет подбираться не методом проб и ошибок, а на основе генетического кода болезни конкретного пациента
Другим, не менее революционным инновационным направлением является использование продвинутых технологий обработки естественного языка (Natural Language Processing — NLP) для интеллектуального анализа неструктурированных электронных медицинских карт (ЭМК). Длина, терминологическая избыточность, хаотичность и обилие аббревиатур в текстовых медицинских записях могут критически затруднять точную интерпретацию истории болезни живым врачом, особенно при наличии сочетанных хронических состояний, накопленных за десятилетия. В одном из недавних ретроспективных кросс-секционных исследований, проведенных на базе крупного итальянского ревматологического центра, был успешно разработан и валидирован классификатор на основе NLP. Алгоритм был обучен различать истинные воспалительные артриты (такие как ревматоидный и псориатический) и невоспалительные ревматические заболевания (остеоартрит, фибромиалгия) исключительно на основе лингвистического анализа 1372 текстовых записей ЭМК (включавших 468 случаев ревматоидного артрита, 732 случая псориатического артрита и 172 случая невоспалительных заболеваний).
Результаты этого эксперимента оказались весьма обнадеживающими и открывающими новые горизонты в скрининге. Обученная модель достигла феноменальной общей точности в 85% в различении этих трех сложных диагностических групп. При этом 74,5% всех случаев были классифицированы алгоритмом искусственного интеллекта с высочайшей степенью уверенности, достигая поразительной точности в 94,6%, тогда как лишь 1,5% случаев система сочла сомнительными и требующими доработки. Важно отметить, что алгоритм не допустил ни единой фатальной ошибки перекрестной классификации между ревматоидным артритом и невоспалительными патологиями, хотя, что вполне ожидаемо с клинической точки зрения, наблюдалось некоторое симптоматическое перекрытие между псориатическим артритом и другими состояниями. Инструменты математической интерпретируемости ИИ (такие как специализированные алгоритмы LIME и SHAP) показали, что главными препятствиями для машины остаются сложный клинический синтаксис и частое использование отрицаний в медицинских текстах (например, "нет данных за воспаление"). Тем не менее, NLP уже сегодня представляет собой мощнейший, безотказный инструмент для массового, потокового скрининга миллионов ЭМК, обеспечивающий исчезающе низкий риск пропуска пациентов с агрессивными воспалительными заболеваниями суставов и помогающий оперативно, без задержек маршрутизировать их к профильным специалистам-ревматологам
Интеграция диагностических модальностей: формирование плана лечения
Комплексные методы диагностики артрита не существуют в вакууме; их конечная, высшая цель — разработка максимально эффективного терапевтического плана. Артрит — это крайне распространенное, но при этом невероятно сложное и гетерогенное заболевание, которое затрагивает миллионы людей и способно катастрофически влиять на базовое качество их жизни. Для огромного числа пациентов эффективное лечение требует строго индивидуализированного плана, скрупулезно адаптированного к их уникальным физиологическим потребностям, генетическому фону и конкретной стадии прогрессирования патологии. Диагностическая визуализация играет в этом длительном процессе критическую, стержневую роль, помогая лечащим врачам принимать глубоко обоснованные, взвешенные решения о выборе начальных вариантов лечения и их своевременной корректировке с течением времени
Регулярный, методичный инструментальный мониторинг состояния суставного аппарата является абсолютно неотъемлемой, обязательной частью грамотной курации больных артритом. Он позволяет лечащим врачам не полагаться исключительно на субъективные жалобы пациента, которые могут искажаться психологическим фактором или привыканием к боли, а видеть объективную картину подавления или, напротив, эскалации воспаления внутри сустава. Опытные радиологи, работающие в тесном, неразрывном тандеме с лечащим ревматологом, интерпретируют сложнейшие результаты визуализации и предоставляют точнейшие морфологические данные для немедленной коррекции доз базисных противоревматических препаратов или принятия решения о переводе пациента на генно-инженерную биологическую терапию.
Сформированный на основе доказательной медицины диагностический алгоритм предполагает строгую последовательность действий. При первичном обращении пациента с жалобами на суставной синдром первоочередной задачей является оперативный лабораторный скрининг воспаления в комбинации с ультразвуковым картированием. При подтверждении воспалительного паттерна в дело вступает тяжелая артиллерия — поиск специфических антител (РФ, АЦЦП) и генетическое типирование на аллель HLA-B27. Если данных все еще недостаточно для уверенного старта агрессивной иммуносупрессивной терапии, или если подозревается глубокое поражение аксиального скелета, назначается магнитно-резонансная томография. Для исключения кристаллических артропатий применяется двухэнергетическая КТ. Только такой всеобъемлющий, мультидисциплинарный подход гарантирует успех.
Заключение
Подводя итог этому всестороннему анализу, можно с уверенностью утверждать, что методы диагностики артрита претерпели за последние десятилетия поистине тектонический, парадигмальный сдвиг. Фокус внимания современной ревматологической науки бесповоротно сместился с запоздалой констатации факта необратимых структурных разрушений на предельно раннюю, предиктивную детекцию молекулярных и клеточных воспалительных изменений. Лабораторные маркеры высочайшей специфичности, такие как антитела к циклическому цитруллинированному пептиду, и достижения молекулярной генетики, в частности типирование антигена HLA-B27, обеспечивают клиницистов мощным фундаментом для точной стратификации рисков развития тяжелейших аутоиммунных патологий.
В то же время инструментальная визуализация достигла небывалых высот разрешения. Доступная ультразвуковая диагностика обеспечивает возможность быстрого, динамического скрининга воспалительной активности непосредственно во время приема пациента , тогда как магнитно-резонансная томография окончательно и бесповоротно закрепила за собой статус эталонного, непревзойденного метода обнаружения скрытых синовитов, отека костного мозга и микроскопических эрозивных изменений мягких и твердых тканей. Внедрение в клиническую практику таких узкоспециализированных методов, как двухэнергетическая компьютерная томография, кардинально меняет фундаментальный подход к дифференциальной диагностике сложных кристаллических артритов. Безусловно, эффективность всех этих классических и инновационных диагностических инструментов в самом ближайшем будущем будет многократно, экспоненциально усилена повсеместным внедрением самообучающихся моделей машинного интеллекта и алгоритмов глубокой обработки естественного языка. Эти цифровые помощники способны анализировать колоссальные, недоступные человеческому разуму массивы медицинских данных ЭМК и выявлять тончайшие предикторы ревматических заболеваний на самых ранних, полностью скрытых доклинических стадиях.
Глубокое, исчерпывающее понимание физических ограничений и клинических преимуществ каждого диагностического метода, а также мастерство их синергетического, комбинированного применения, позволяет врачам формировать оптимальные, персонализированные планы ведения пациентов. Именно такой подход способен радикально снизить риск тяжелой инвалидизации и значимо, ощутимо повысить качество жизни больных с тяжелейшими патологиями опорно-двигательного аппарата. С учетом угрожающего, неуклонного роста заболеваемости воспалительными и дегенеративными артритами на фоне глобальных демографических сдвигов, экологических проблем и эпидемии метаболических нарушений, грамотное владение всем арсеналом доступных методов становится не просто желательным, а жизненно необходимым фактором успеха в реалиях современной медицины. Усилия медицинского сообщества должны быть направлены на повсеместное внедрение этих технологий, обучение специалистов и обеспечение максимальной доступности высокотехнологичной помощи для каждого пациента, нуждающегося в защите своих суставов и сохранении свободы движения